Естер проти ефіру

Зміст
Ефір та ефір - це органічні молекули з атомами кисню. Обидва мають ефірну зв'язок, який становить –O-. Ефіри мають групу –СОО. Один атом кисню пов'язаний з вуглецем подвійним зв’язком, а інший кисень пов'язаний одинарним зв’язком. Оскільки до атома вуглецю пов'язано лише три атоми, він має трикутну площинну геометрію навколо нього. Далі, атом вуглецю є sp2гібридизований.
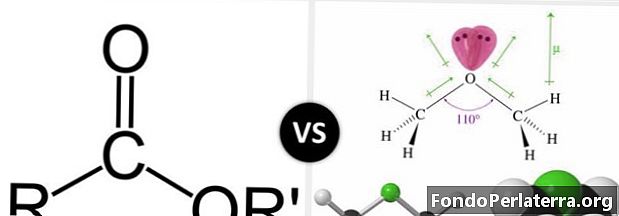
Карбоксильна група - це функціональна група, що часто зустрічається в хімії та біохімії. Ця група є батьківською родиною спорідненого сімейства сполук, відомих як ацилові сполуки. Ацилові сполуки також відомі як похідні карбонової кислоти. Ефір - це таке похідне карбонової кислоти. Ефір з'єднання має зв'язок вуглець-карбоніл-кисень, тоді як ефірна сполука має зв'язок вуглець-кисень-вуглець.
Зміст: Різниця між ефіром та ефіром
- Що таке Естер?
- Що таке ефір?
- Ключові відмінності
- Відео Пояснення
Що таке Естер?
Ефіри мають загальну формулу RCOOR '. Складні ефіри утворюються реакцією карбонової кислоти зі спиртом. Ефіри називають, спочатку записуючи назви спиртних частин. Тоді назва, що походить від кислотної частини, пишеться із закінченням -їли або -оат.

Що таке ефір?
Прості ефіри мають функціональну групу ROR, наприклад Етоксипропан. Ефір - це сполука, яка має вуглецево-вуглецеву зв’язок. Прості ефіри можуть бути отримані міжмолекулярною дегідратацією спиртів. Зазвичай це відбувається при більш низькій температурі, ніж дегідратація до алкену.

Ключові відмінності
- Ефіри є похідними карбонової кислоти і мають групу –СОО. Ефіри мають –О- функціональну групу.
- Ефір має карбонільну групу, прилеглу до -O-кисню, але ефір такого не має.
- Ефіри мають стільки характерних запахів.
- Ефіри легко гідролізуються з утворенням спирту та карбонової кислоти на відміну від ефірів.
- Ефіри мають функціональну групу RCOOR з подвійною зв'язком С до одного з Os і одинарною зв'язком з іншою О. Наприклад, Етилэтаноат. Тоді як ефіри мають функціональну групу ROR, наприклад Етоксипропан
- Ефір - це сполука, яка має вуглецево-вуглецеву зв’язок. Прикладом ефіру є етоксилат. З'єднання нижче - лаурет 5. Ефір, з іншого боку, являє собою сполуку, яка має вуглець-карбоніло-кисневий вуглецевий зв’язок.
- Основна характеристика, яка відрізняє ефір від ефіру, - це їхня різна структура. З'єднання, відоме як складний ефір, має вуглець-карбоніло-кисневу зв'язок, тоді як ефірна сполука має зв'язок вуглець-кисень-вуглець.
- Ефіри - це полярні сполуки, але вони не мають здатності утворювати міцні водневі зв’язки один з одним через відсутність водневої зв'язку з киснем. В результаті складні ефіри мають більш низькі температури кипіння порівняно з кислотами або спиртами з аналогічною молекулярною масою. Прості ефіри можуть бути отримані міжмолекулярною дегідратацією спиртів. Зазвичай це відбувається при більш низькій температурі, ніж дегідратація до алкену. Синтез Вільямсона - ще один метод отримання несиметричних ефірів.





